Fim da Exclusividade e Chegada de Alternativas
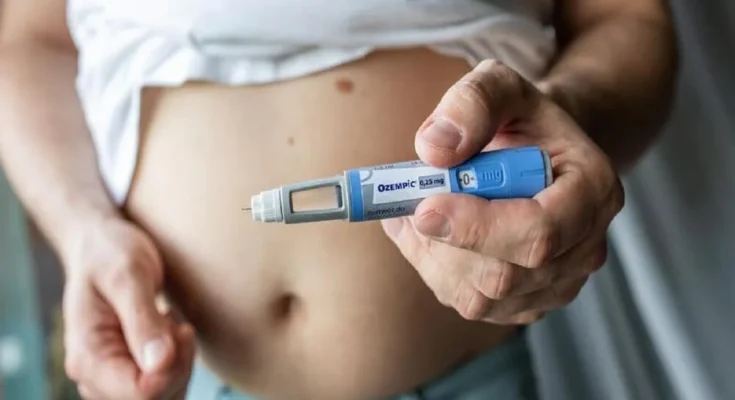
A patente da semaglutida, princípio ativo de medicamentos como Ozempic e Rybelsus, conhecidos popularmente como ‘canetas emagrecedoras’, expira no Brasil nesta sexta-feira (20). Essa data marca o fim da exclusividade da empresa dinamarquesa Novo Nordisk na produção e comercialização desses medicamentos no país, abrindo caminho para o surgimento de versões mais acessíveis no mercado farmacêutico.
Atualmente, a Agência Nacional de Vigilância Sanitária (Anvisa) já analisa oito processos para novos medicamentos com o mesmo princípio ativo. Desses, dois pedidos de registro de semaglutida sintética estão em fase de exigência, aguardando a apresentação de dados complementares pelas empresas. O prazo para essa resposta se estende até o final de junho, o que impede a definição de prazos para a conclusão do processo. Além disso, um produto biológico está em análise e outro aguarda o início da avaliação.
Desafios Técnicos na Produção de Análogos Sintéticos
Medicamentos à base de semaglutida registrados no Brasil são classificados como produtos biológicos. No entanto, os novos pedidos em análise incluem tanto biossimilares (obtidos por via biológica) quanto análogos sintéticos (obtidos por síntese química). Diferente dos medicamentos genéricos, os produtos biológicos não possuem essa categoria de registro, devendo se enquadrar nas classificações de biossimilar ou análogo sintético.
A Anvisa ressalta que a avaliação de análogos sintéticos de semaglutida representa um desafio técnico global. Até o momento, as principais agências reguladoras de medicamentos no mundo, como as do Japão, Europa e Estados Unidos, não registraram análogos sintéticos da semaglutida. Isso se deve à necessidade de avaliar esses produtos sob parâmetros tanto de fármacos sintéticos quanto de biológicos, considerando riscos como resíduos de solventes e catalisadores, além de potenciais reações de imunogenicidade e formação de agregados.
Foco da Anvisa: Segurança e Eficácia
A agência reguladora tem como foco principal a avaliação rigorosa de pontos como ensaios de impurezas, formação de agregados, garantia de esterilidade e imunogenicidade. O objetivo é assegurar que os novos medicamentos não causem reações imunes indesejadas, como o desenvolvimento de anticorpos que poderiam levar à ineficácia do tratamento ou reações mais graves para os pacientes.
Decisão Judicial e o Futuro da Semaglutida no Brasil
A decisão que impulsiona a chegada de alternativas mais baratas foi tomada em janeiro pela Quarta Turma do Superior Tribunal de Justiça (STJ). O tribunal negou a prorrogação do prazo de vigência das patentes de Ozempic e Rybelsus, a pedido da Novo Nordisk. A empresa alegava mora administrativa na análise das patentes pelo Instituto Nacional da Propriedade Industrial (Inpi). Contudo, o STJ manteve o entendimento consolidado pelo Supremo Tribunal Federal (STF) de que o prazo de vigência de uma patente é de 20 anos a contar do depósito do pedido, sem possibilidade de prorrogação judicial por atrasos administrativos.
Fonte: www.brasildefato.com.br